1. sục 8,96 lít khí co2 đktc vào 300 g naoh 8 % . Tính C% của dd sau pư
Tính nồng độ mol của các chất tan trong dd thu đc sau mỗi thí nghiệm sau đây. Biết các pư xảy ra hoàn toàn, V dd thay đổi k đáng kể.
a. Sục 448ml khí CO2 (đktc) vào 400ml dd Ca(OH)2 0,02M
b. Sục 4,032 lít khí SO2 (đktc) vào 200ml dd Ba(OH)2 1M
a. \(n_{CO_2}=0,02\left(mol\right);n_{Ca\left(OH\right)_2}=0,008\left(mol\right)\Rightarrow n_{OH^-}=0,016\\ Tacó:\dfrac{n_{OH^-}}{n_{CO_2}}=\dfrac{0,016}{0,02}=0,8\Rightarrow ChỉtạoCa\left(HCO_3\right)_2,CO_2dư\\ 2CO_2+Ca\left(OH\right)_2\rightarrow Ca\left(HCO_3\right)_2+H_2O\\ n_{Ca\left(HCO_3\right)_2}=n_{Ca\left(OH\right)_2}=0,016\left(mol\right)\\ \Rightarrow CM_{Ca\left(HCO_3\right)_2}=\dfrac{0,016}{0,4}=0,04M\)
\(b.n_{SO_2}=0,18\left(mol\right);n_{Ba\left(OH\right)_2}=0,2\left(mol\right)\Rightarrow n_{OH^-}=0,4\left(mol\right)\\Tacó:\dfrac{n_{OH^-}}{n_{CO_2}}=\dfrac{0,4}{0,18}=2,22\Rightarrow Ba\left(OH\right) _2dư\\ SO_2+Ba\left(OH\right)_2\rightarrow BaCO_3+H_2O\\ n_{Ba\left(OH\right)_2dư}=0,2-0,18=0,02\left(mol\right)\\ \Rightarrow CM_{Ba\left(OH\right)_2dư}=\dfrac{0,02}{0,2}=0,1M\)
Sục 8.96 lít khí CO2 (ở đktc) vào 200ml dd NaOH 2M. Tính nồng độ mol của dd thu đc
![]()
tính khối lượng các chất có trong dd sau phản ứng trong các trường hợp sau:
a) sục từ từ 2,24 lít CO2 vào 500ml dd NaOH 0,2M
b) dẫn 11,2 lít SO2 vào dd chứa 84 g KOH
c) sục 13,2g CO2 vào 500 ml Ca(OH)2 0,4M biết thể tích các khí đo ở đktc
a) nco2=v/22.4=0.1 mol
500ml=0.5l
=> nNaoh=Cm.v=0.2 . 0.5=0.1 mol
lập tỉ lệ:
nNaoh/nCo2=0.1/0.1=1
=> sảy ra phương trình
Naoh + co2 ->nahco3
mCo2=n.M=4.4 (g)
mNaoh=n.M=4 (g)
adđlbtkl ta có
mCo2 + mNaoh = mNahco3
=>mNahco3=8.4 (g)![]()
Ta có: \(\left\{{}\begin{matrix}n_{CO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\n_{Ba\left(OH\right)_2}=0,5\cdot0,3=0,15\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\) Tạo muối trung hòa
PTHH: \(Ba\left(OH\right)_2+CO_2\rightarrow BaCO_3\downarrow+H_2O\)
Vì Ba(OH)2 dư nên tính theo CO2
\(\Rightarrow n_{BaCO_3}=0,1\left(mol\right)\) \(\Rightarrow m_{BaCO_3}=0,1\cdot197=19,7\left(g\right)\)
Nung nóng m gam hh gồm A1 và Fe3O4 trong điều kiện không có không khí. Sau khi pư xảy ra hoàn toàn, thu được hh rắn X. Cho X t/d với dd NaOH (dư) thu được dd Y, chất rắn Z và 3,36 lít khí H2 (ở đktc). Sục khí CO2 (dư) vào dd Y, thu được 39 gam kết tủa. Giá trị của m là
A. 45,6.
B. 48,3.
C. 36,7.
D. 57,0.
Đáp án B
Rắn X phải có A1 dư vì chỉ có A1 mới phản ứng với dung dịch NaOH tạo khí H2. Mặt khác do phản ứng hoàn toàn nên Fe3O4 hết.
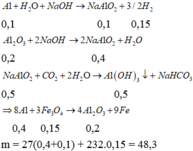
Cho 6 lít hh CO2 và N2 (đktc) đi qua dd NaOH . sau pư thu đc dd X. cho BaCl2 vào X được 2,955 g kết tủa, lọc bỏ kết tủa được dd Y. cho Ba(OH)2 dư vào Y được 11,82 g kết tủa. tính % V(CO2) trog hh ban đầu
Khi cho hỗn hợp khí vào dung dịch NaOH thì chỉ có khí CO2 phản ứng với NaOH ( Chú ý đề thiếu, NaOH phải dư nhé!)
\(CO_2+2NaOH--->Na_2CO_3+H_2O\) (1)
0,075 <-----------------------------------------0,075 (mol)
Dung dịch X là Na2CO3 .
\(Na_2CO_3+BaCl_2--->BaCO_3\downarrow+2NaCl\)(2)
0,015 <----------------------------------------0,015 (mol)
Kết tủa là BaCO3, dung dịch Y gồm NaCl và có thể là BaCl2 dư hoặc Na2CO3 dư
Cho dung dịch Y vào Ba(OH)2 xuất hiện kết tủa nên dung dịch Y sẽ là có Na2CO3 dư.
\(Na_2CO_3+Ba\left(OH\right)_2--->BaCO_3\downarrow+2NaOH\) (3)
0, 06 <----------------------------------------- 0,06 (mol)
Ta có: \(n_{BaCO_3\left(2\right)}=\frac{2,955}{137+12+16.3}=0,015\left(mol\right)\)
\(n_{BaCO_3\left(3\right)}=\frac{11,82}{137+12+16.3}=0,06\left(mol\right)\)
=> \(n_{Na_2CO_3\left(X\right)}=0,015+0,06=0,075\left(mol\right)\)
=> \(n_{CO_2}=0,075\left(mol\right)\)=> \(V_{CO_2}=0,075.22,4=1,68\left(l\right)\)
=> \(\%V_{CO_2}=\frac{1,68}{6}.100\%=28\%\)
Sục 1,344 lít khí CO2 ( ĐKTC ) vào 300 ml dd Tính khối lượng muối thu được sau phản ứng. |
Please help me ![]() . Ai best hoá ib zalo vs tui hộ nha, nhắn tin zui zui vs nhận tui lm đồ đệ đc hong
. Ai best hoá ib zalo vs tui hộ nha, nhắn tin zui zui vs nhận tui lm đồ đệ đc hong ![]() ----0938689561------
----0938689561------![]()
Sục V lít khí CO2 ở đktc vào 0.2 lít dd Ca(OH)2 0.5 M thu được 2.5 g kết tủa. tính V?
Ta có : nCa(OH)2 = 0,2 . 0,5 = 0,1 (mol)
n CaCO3 = 2,5 : 100 = 0,025 mol
Khi sục V lít khí CO 2 vào dung dịch Ca(OH)2 thì có thể xảy ra 2 trường hợp sau :
Trường hợp 1: Ca(OH)2 tác dụng vừa đủ hoặc dư , còn khí CO2 tác dụng hết . Chỉ xảy ra phản ứng sau :
CO2 + Ca(OH)2 = CaCO3 + H2O ( 1 )
0,025 < ----- 0,025 <-----0,025 mol
số mol Ca(OH)2 phản ứng = 0,025 mol < 0,1 mol (phù hợp )
Vậy n CO2 là 0,025 mol => V = 0,025 . 22,4 = 0,56 lít
Trường hợp 2 : Ca(OH)2 tác dụng hết , khí CO2 có dư sau phản ứng ( 1 ) . Trước hết xảy ra phản ứng ( 1 )
CO2 + Ca(OH)2 = CaCO3 + H2O ( 1 )
0,1 mol <----0,1 mol -----> 0,1 mol
Sau khi (1) kết thúc , lượng Ca(OH)2 cũng hết , khí cacbonic còn dư sau pư sẽ tiếp tục phản ứng với muối CaCO3 tạo thành ( làm giảm bớt lượng kết tủa sau pư 1 )
CO2 + H2O + CaCO3 = Ca(HCO3)2 (2)
0,075 mol <------------ 0,1 - 0,025 = 0,075
Vậy tổng số mol khí CO 2 thổi vào là 0,1 + 0,075 = 0,175 mol
=> V = 0,175 . 22,4 = 3,92 lít
\(n_{Ca\left(OH\right)_2}=0,5.0,2=0,1\left(mol\right)\)
PTHH : CO2 + Ca(OH)2 -----> CaCO3 + H2O
=> \(n_{CaCO_3}=\frac{2,5}{100}=0,025\left(mol\right)\)
Ta có \(\frac{n_{Ca\left(OH\right)_2}\left(\text{bài ra}\right)}{n_{Ca\left(OH\right)_2}\left(\text{phương trình}\right)}=\frac{0,1}{1}>\frac{n_{CaCO_3}\left(\text{bài ra}\right)}{n_{CaCO_3}\left(\text{phương trình}\right)}=\frac{0,025}{1}\)
=> CaCO3 phản ứng hết , Ca(OH)2 dư
Suy ra nCO2 = 0,025 mol
=> VCO2 = 0,025 . 22,4 = 0,56 (lít)
trong trường hợp,ta không bận tâm pư tạo muối nào vì ta biết muối CaCO3 kết tủa nên sản phẩm không
nCa(OH)2 = 0,2 . 0,5 = 0,1 (mol)
n CaCO3 = 2,5 : 100 = 0,025 mol
Khi sục V lít khí CO 2 vào dung dịch Ca(OH)2 thì có thể xảy ra 2 trường hợp sau :
Trường hợp 1: Ca(OH)2 tác dụng vừa đủ hoặc dư , còn khí cacbonic tác dụng hết . Chỉ xảy ra phản ứng sau :
CO 2 + Ca(OH)2 = CaCO 3 + H2O ( 1 )
0,025 < ----- 0,025 <-----0,025 mol
số mol Ca(OH)2 phản ứng = 0,025 mol < 0,1 mol (phù hợp )
Vậy n CO 2 là 0,025 mol => V = 0,025 . 22,4 = 0,56 lít
Trường hợp 2 : Ca(OH)2 tác dụng hết , khí CO 2 có dư sau phản ứng ( 1 ) . Trước hết xảy ra phản ứng ( 1 )
CO 2 + Ca(OH)2 = CaCO 3 + H2O ( 1 )
0,1 mol <----0,1 mol -----> 0,1 mol
Sau khi (1) kết thúc , lượng Ca(OH)2 cũng hết , khí cacbonic còn dư sau pư sẽ tiếp tục phản ứng với muối CảCO tạo thành ( làm giảm bớt lượng kết tủa sau pư 1 )
CO2 + H2O + CaCO3 = Ca(HCO3)2 (2)
0,075 mol <------------ 0,1 - 0,025 = 0,075
Vậy tổng số mol khí CO 2 thổi vào là 0,1 + 0,075 = 0,175 mol
=> V = 0,175 . 22,4 = 3,92 lít
Chúc em học tốt !!!
1. Hấp thụ hoàn toàn 2,24 lít CO2 (đktc) vào 100ml dd NaOH. Sau phản ứng nung từ từ dung dịch thu đc 9,5g muối khan. Tính nồng độ mol của dd NaOH đã dùng
2. Người ta dẫn 2,24 lít CO2 qua bình đựng dd NaOH. Khí CO2 bị hấp thụ hoàn toàn. Sau phản ứng thu được muối nào tạo thành? khối lượng là bn?
1.nCO2=0,1 (mol )
TH1: Số mol của CO2 dư => Khối lượng muối khan tối đa tạo được là:
mmuối=0,1.84=8,4<9,5 (loại )
TH2: CO2 hết
Gọi số mol CO2 tạo muối Na2CO3;NaHCO3 lần lượt là x, y
2NaOH+CO2→Na2CO3+H2O
NaOH+CO2→NaHCO3
Ta có : \(\left\{{}\begin{matrix}x+y=0,1\\106x+84y=9,5\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,05\\y=0,05\end{matrix}\right.\)
⇒nNaOH=2.0,05+0,05=0,15 (mol)
⇒CMNaOH=\(\dfrac{0,15}{0,1}\)=1,5M
Câu 2 thật ra anh thấy chưa chặt chẽ nha!
2. Vì CO2 bị hấp thụ hoàn toàn
=> CO2 hết, NaOH dư
nCO2 = 0,1 (mol)
CO2 + 2NaOH -------> Na2CO3 + H2O
\(n_{Na_2CO_3}=n_{CO_2}=0,1\left(mol\right)\)
=> \(m_{Na_2CO_3}=0,1.106=10,6\left(g\right)\)